Souhrn
Přidání dlouhodobě působícího antagonisty cholinergních receptorů do terapie těžkého astmatu, které je pod nedostatečnou kontrolou, vede ke zlepšení kontroly nad onemocněním. Novinkou v léčbě je fixní trojkombinace (duální bronchodilatace a inhalační kortikosteroid) v jednom inhalátoru, produkující konstantně veliké jemné částice s dosahem do oblasti drobných dýchacích cest. Dobrý terapeutický efekt, bezpečnost terapie při snadné manipulaci s inhalátorem zlepšuje kvalitu života a posiluje complianci nemocných k léčbě.
Klíčova slova: těžké astma, IKS, duální bronchodilatační léčba, trojkombinace
Alena Vlachová, Libor Fila
Plicní klinika 2. LF a FN Motol, Praha
Úvod
Bronchiální astma je heterogenním syndromem, jehož klinický obraz je vysoce variabilní a jeho terapie se odvíjí od jednotlivých fenotypů astmatu. Základním úkolem léčby je dosáhnout kontroly nad onemocněním a zabránit jeho progresi, zejména vzniku a opakování exacerbací s poklesem ventilačních funkcí a přestavbou dýchacích cest. Exacerbace vždy znamenají propad v celkovém stavu nemocného s následkem zhoršení dechových funkcí, nutnosti navýšení jak bronchodilatační, tak protizánětlivé léčby s cílem stabilizace stavu i za cenu vedlejších efektů terapie. Opakované exacerbace tak vedou ke snížení kvality života nemocných a ke zvýšení mortality. Celkekm 95–98 % nemocných profituje z obvyklé kombinační terapie inhalačními kortikosteroidy (IKS) pro stabilizaci zánětu v dýchacích cestách s bronchodilatační léčbou dlouhodobě účinkujícími beta2-agonisty (LABA). Zbývající skupina je sice počtem malá, nicméně svým významem závažná, ať již z medicínského, či ekonomického hlediska. Jedná se o nemocné, jejichž astma je pod nedostatečnou kontrolou, jsou na střední až vysoké dávce IKS, nejednou s nutností nasazení systémové kortikoterapie. Z hlediska pětistupňové úrovně terapie dle doporučení GINA (Globální strategie pro léčbu a prevenci astmatu) jsou to pacienti na stupni 4 a 5 (1, 2).
Nové možnosti léčby
Kvalita života těchto nemocných je nízká vzhledem k omezení četnými exacerbacemi, dlouhodobě dysfunkčním stavem plic, špatnou kondicí, psychickou nadstavbou spolu s vedlejšími efekty terapie. Pouze asi jen 2 % nemocných z této skupiny můžeme dle jejich fenotypu nabídnout biologickou léčbu, proto je nutno efektivně využít to, co je v terapii astmatu k dispozici.
Na podkladě provedených studií mezi lety 2008–2014 bylo možné dle doporučení GINA 2014 (v České republice od roku 2015) doplnit léčbu u nemocných s nedostatečnou kontrolou nad onemocněním (dle GINA stupeň 4 a 5) o dlouhodobě působící antagonisty muskarinových receptorů (LAMA).(1, 2). Doporučení je logické, duální bronchodilatační léčba vede k navýšení ventilačních parametrů při nižších dávkách jednotlivých léků, je využit aditivní efekt jednotlivých léků v kombinaci, terapie je tedy bezpečnější.
Prvním povoleným lékem bylo tiotropium (Spiriva Respimat). Tiotropium je cholinergikum (antagonista muskarinových receptorů) s ultra dlouhodobým účinkem (U LAMA) (1, 2, 3). Cílem bylo stabilizovat dechové funkce, zabránit poklesu poklesu úsilovně vydechnutého objemu vzduchu za 1 vteřinu (FEV 1 ), redukovat počet exacerbací a získat tak kontrolu nad onemocněním. V současné době použití tiotropia v terapii dle doporučení GINA 2020 přetrvává, nicméně vzhledem k současným terapeutickým možnostem již nebude jediné.
V terapii chronické obstrukční choroby bronchopulmonální (CHOPN) již fixní trojkombinaci (4,5,6,7) využíváme s dobrým efektem u fenotypu častých exacerbací a překryvného syndromu CHOPN s astmatem (ACO). K dispozici jsou dva léky: Trimbow – obsahující beklometason dipropionát, formoterol furoát, glykopyrronium (BDP/FF/G) v pMDI inhalátoru via systém Modulite (8) a Trelegy – obsahující flutikason furoát, umeklidinium bromid a vilanterol (FF/Umec/Vil) via inhalátor Ellipta (9, 10). Lze tedy předpokládat, že je-li fixní trojkombinace efektivní pro uvedené fenotypy CHOPN, proč by neměla být stejně efektivní u bronchiálního astmatu? Na tuto otázku odpovídají současné studie fixních trojkombinací.
Předkládáme výsledky dvou studií fáze 3, které hodnotí efekt a bezpečnost trojkombinace (BDP/FF/G) v jednom inhalátoru via systém Modulite u nemocných s těžkým astmatem pod nedostatečnou kontrolou ve srovnání s kombinací BDP/FF ve studii TRIMARAN a ve studii TRIGGER, která měla navíc v doplněné 3. otevřené větvi (open-label) kombinaci BDP/FF + tiotropium separátně via Respimat v dávce 5 µg (11). Tato dvojitě zaslepená, randomizovaná, aktivně kontrolovaná studie trvala celkem 52 týdnů. Bylo do ní zařazeno celkem 1 155 pacientů (171 center z 16 zemí) ve studii TRIMARAN a 1 437 pacientů (221 center ze 17 zemí) ve studii TRIGGER. Jednalo se o nemocné s minimálně 1 rok potvrzenou diagnózou astmatu, nekuřáky či nerecentní exkuřáky ve věku mezi 18–75 lety, s pozitivním bronchodilatačním testem pro salbutamol 400 µg, bez závažných komorbidit, bez biologické terapie, ventilačně se středně těžkou obstrukcí. Cca třetina účastníků měla obezitu 1. stupně s indexem tělesné hmotnosti (BMI) >30 (30 % ve studii TRIMARAN a 36 % ve studii TRIGGER). Všichni nemocní měli ≥1 středně těžkou až těžkou exacerbaci v předchozím roce, jednalo se tedy o nemocné s onemocněním pod nedostatečnou kontrolou. Ve studii TRIMARAN byli nemocní s nižší dávkou IKS (100 µg BDP) proti studii TRIGGER, kde byla dávka dvojnásobná (BDP 200 µg). Dávka bronchodilatačního léku (FF 6 µg) byla v obou studiích stejná, tak jako dávka anticholinergika (10 µg G). Obě studie srovnávaly fixní trojkombinace s duální kombinací BDP/FF. Veškerá medikace byla podávána 2× denně po 2 dávkách kromě 1× denně podávaného tiotropia.

Primárním cílem bylo prokázat ve 26. týdnu (v polovině studie) zvýšení FEV 1 před ranní aplikací léku a vliv léku na počet středně těžkých až těžkých exacerbací. Dále byla hodnocena změna FEV 1 v rámci 26 týdnů a průměrná hodnota ranní vrcholového výdechového průtoku (PEF) (obr. 1) spolu s mírou středně těžkých a těžkých exacerbací v obou studiích (obr. 2).
Druhotným cílem bylo sledování změn FEV 1 (změny ≥100 ml od vstupní FEV 1 před ranní medikací) v 26. a 52. týdnu, změny hodnot plochy pod křivkou mezi 0. a 3. hodinou po podání léku (AUC 0-3 h ), denní variabilitu PEF, včetně posouzení ranních a večerních hodnot, čas do první exacerbace a její tíži. Dále byl hodnocen počet exacerbací, množství záchranné medikace, jakož i počet asymptomatických dnů během celé studie.
Subjektivní stav byl sledován pomocí dotazníku Asthma Control Questionnaire-7 (ACQ-7), jednak v rámci všech kontrol jako srovnání se vstupními hodnotami v 26. + 52. týdnu studie, jako signifikantní je hodnocena redukce o 0,5 proti vstupním hodnotám. Dalším kritériem byla bezpečnost prokázané medikace.
Obě studie prokazují superioritu trojkombinace BDP/FF/G proti dvojkombinaci BDP/FF. Ventilačně došlo ke zvýšení FEV 1 ve 26. týdnu o 57 ml (95 %CI 15–99 p = 0,0080) ve studii TRIMARAN a o 73 ml (26–120, p = 0,0025) ve studii TRIGGER (obr. 3).
Středně těžké a těžké exacerbace byly redukovány o 15 % u studie TRIMARAN a o 12 % u studie TRIGGER, což vztaženo na celkový počet nemocných, je pozitivním výsledkem.

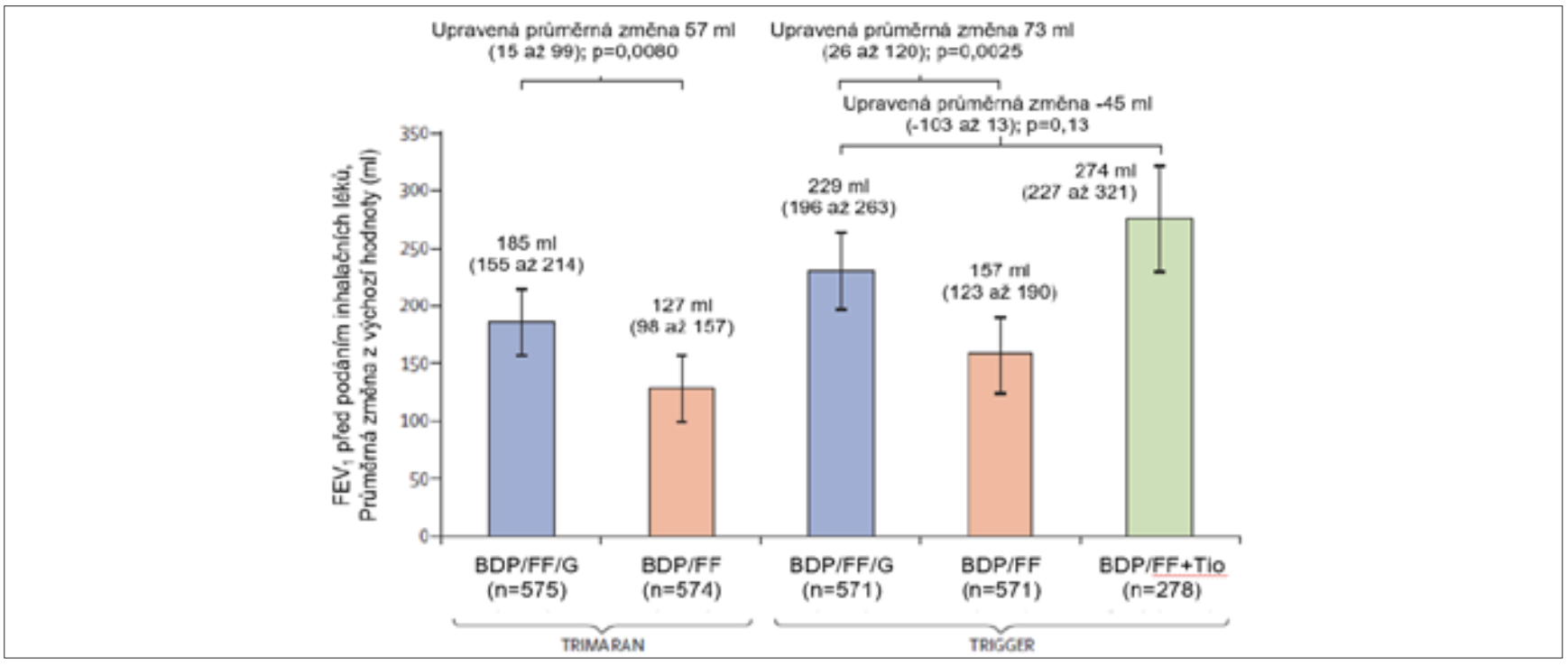
Obr. 3: Primární cíl studií TRIMARAN a TRIGGER. Nárůst hodnoty FEV 1 dle jednotlivých skupin
Celkově se lépe dařilo nemocným s vyšší dávkou IKS ve studii TRIGGER. Prodělané exacerbace v obou studiích byly mírné. Významně také poklesl čas do první střední nebo těžké exacerbace o 16 % a 20 % ve studii TRIMARAN a TRIGGER (obr. 4 a 5).
Rozdíly mezi fixní trojkombinací a fixní dvojkombinací BDF/FF s tiotropiem v separátním inhalátoru nebyly významné. Vedlejší efekty terapie byly mírné, čtyři nemocní (1 % z populace) ve studii TRIMARAN, tři (1 % z populace) ve studii TRIGGER měli kardiovaskulární příhodu, která však nebyla v návaznosti na léčbu, zaznamenané příčiny úmrtí nebyly shledány jako související se studijní medikací.
Studijní medikace, tedy jak dvojkombinace BDP/FF tak trojkombinace BDP/FF/G, jsou podávány inhalačním systémem Modulite, který zajišťuje tvorbu extrafine částic k inhalaci. Jejich velikost je mezi 1,4–1,5 µm středního aerodynamického průměru (MMAD), což umožňuje průnik dýchacím stromem až do oblasti drobných dýchacích cest, tedy do oblasti distálně od terminálních bronchiolů s průměrem dýchacích cest do 2 µm (12, 13). Oblast malých dýchacích cest je v centru našeho zájmu, protože je rozsáhlá, zaujímá cca 90 % objemu plic a za normálních okolností tvoří jen 10 % rezistence. Nicméně k vysokému podílu hladké svaloviny je schopna generalizovaného bronchospasmu a zásadně se tak podílí na nárůstu odporu dýchacích cest, což vede k masivní periferní hyperinflaci s jejími důsledky. Z tohoto důvodu je velmi důležité dostat medikaci co nejdále do periferie dýchacích cest, což použití extrafine částic v inhalátoru umožňuje. I když víme, že receptorů pro anticholinergika směrem do periferie ubývá, v celkovém kontextu lze předpokládat, že jejich podporou bronchodilatace se dostane adekvátní dávka léku k periferním receptorům beta2-agonistů a kortikosteroidů do oblasti drobných dýchacích cest. Tímto způsobem stabilizujeme v celém bronchiálním stromu jak zánětlivou složku astmatu, tak průsvit dýchacích cest, chráníme architekturu před remodelací a nemocného před dušností z exacerbací. Obdobný design mají studie dvou dalších možných fixních trojkombinací.
___

Bezpečnost a efektivita trojkombinace indacaterol, mometasone furoát, glykopyrronium (IND/MF/G) v přípravku Enerzair (via Breezhaler) byla posuzována v randomizované, dvojitě zaslepené studii fáze 3 (IRIDIUM) (14, 15). Indacaterol (U-LABA) a mometasone jsou léky s ultradlouhodobým efektem účinku, glycopyrronium je v tomto případě podáváno lze podat jako U-LAMA jen jednou denně. Enerzair v podání 1× denně prokázal v 26. týdnu 52týdenní studie klinicky významné zlepšení plicních funkcí proti kombinaci dlouhoi ultra dlouhoúčinkujícího beta 2 agonisty s inhalačním kortikosteroidem (U-LABA/IKS: IND/MF, LABA/IKS: SAL/ FLU P), sekundárním endpointem byl pokles počtu exacerbací proti dvojkombinacím IKS/LABA. Ve studii ARGON byla srovnávána fixní trojkombinace (IND/MF/G) s různou dávkou IKS (MF 80 µg a 160 µg) proti kombinaci SAL/FLU P s volně podávaným tiotropiem, kdy efekt byl srovnatelný, nicméně prioritní byla kombinace s nižší dávkou IKS (16).
___
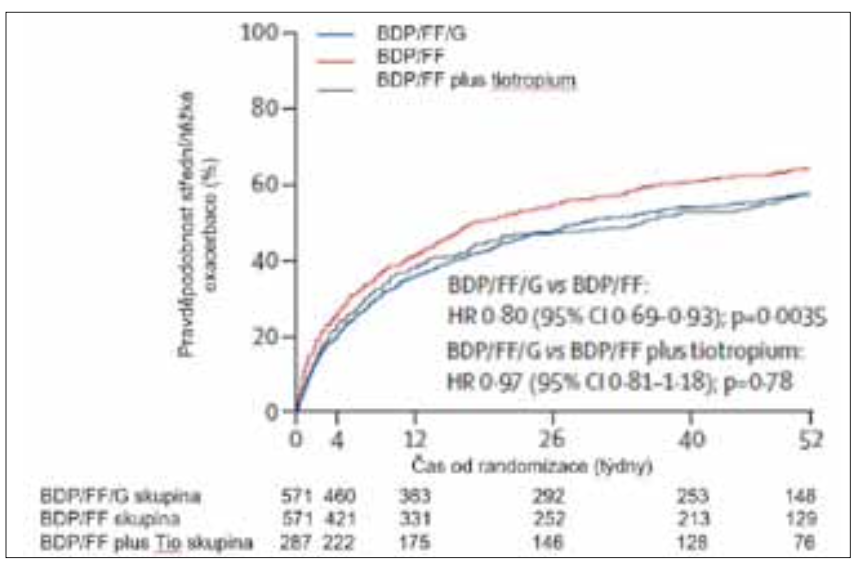
Obr. 5: Čas do první střední nebo těžké exacerbace ve studii TRIGGER
___
Z léčby CHOPN je známa třetí z fixních trojkombinací: flutikason furoát, umeklidinium, vilanterol (FLU F/Umec/VI) v přípravku Trelegy podávaný 1× denně. Studie CAPTAIN opět randomizovaná, dvojitě zaslepená, fáze 3 A hodnotila efekt různých dávek jak IKS (100 či 200 µg FF), tak anticholinergika (Umec v dávce 31,25 µg nebo 62,5 µg) s fixní dávkou 25 µg VI proti IKS/LABA (FF 100 µg/VI) (17). Proti dvojkombinaci IKS/LABA je nárůst FEV ve všech 4 podskupinách, redukce počtu exacerbací je lepší1 s vyšší dávkou IKS a u nemocných s vyšší eozinofilií periferního krevního obrazu a vyšší hladinou vydechovaného oxidu dusíku, design studie však v současné době nepodporuje užití tohoto léku pro astma.
___
Závěr
Proč tedy indikovat fixní trojkombinaci? Je efektivní a bezpečná – v kombinační léčbě hrozí menší nebezpečí předávkování při aditivním působení různých mechanismů účinku. Je jednoduchá a tím se zvyšuje compliance nemocného, zejména zjistí-li, že se mu daří lépe. Nácvik aplikace a kontrola správné manipulace je v dlouhodobé léčbě snadnější pro jeden konkrétní inhalátor jak pro pacienta, tak pro jeho ošetřujícího lékaře – je zde jistota, že doporučovanou medikaci bude nemocný užívat tak, jak je potřeba.
A který inhalátor použít? Vzhledem k léčbě CHOPN máme dostatek zkušeností s kombinací BDP/FF/G v přípravku Trimbow, je tedy jednoduché ho využít pro léčbu astmatu. Kombinaci IND/MF/G v přípravku Enerzair je nutno vyzkoušet v klinické praxi, i když zkušeností s inhalátorem Breezhaler je dostatek.
Použité anticholinergikum v obou trojkombinačních lécích je stejné – glycopyrronium. Je možné je použít v dávkování jak jednou (IND/MF/G), tak dvakrát denně (BDP/FF/G) (18). Převážná vazba na M3 receptory cholinergních nervových vláken jej předurčuje jako bezpečnou složku kombinovaných reparátů. Proti tiotropiu má cca 5x rychlejší nástup účinku (během 5–15 minut), což může být prospěšné u nemocných s večerními až nočnímu obtížemi v podávání 2× denně (19).
Závěrem je nutné říci, že fixní trojkombinace duální bronchodilatací LABA/LAMA s protizánětlivou složkou inhalačního kortikosteroidu v léčbě astmatu je dalším krokem ke zjednodušení a zkvalitnění terapie.
Práce byla podpořena projektem Ministerstva zdravotnictví koncepčního rozvoje výzkumné organizace 00064203 FN Motol.
___
Prohlášení o střetu zájmů:
Autoři práce prohlašují, že v souvislosti s tématem, vznikem a publikací tohoto článku nejsou ve střetu zájmu a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou.
lit ER atu R a
1. 2020 GINA Main Report – Global Initiative for Asthma (Internet). GINA 2020 (cited 2021Apr20). Dostupné z: https://ginasthma. org/gina-reports/
2. Teřl M, Čáp P, Dvořáková R, et al. Doporučený postup diagnostiky a léčby bronchiálního astmatu. Geum 2015.
3. Krčmová I, Sýkora D. Tiotropium bromid v léčbě bronchiálního astmatu. Remedia 2015; 25:315-318.
4. Pocket guide to COPD, diagnosis, management, and prevention. A guide for health care professionals. Global initiative for chronic obstructive lung disease, 2020. Dostupné z: https://goldcopd.org/ wp-content/uploads/2019/11/GOLD-Pocket-Guide-2020-final-wms.pdf
5. Zheng Y, Zhu J, Liu Y, et al. Triple therapy in the management of chronic obstructive pulmonary disease: systematic review and meta-analysis. British Med J 2018; 6(363):k4388, https://doi. org/10.1136/bmj.k4388
6. Lipson DA, Barnhart F, Brealey N, et al. IMPACT Investigators.
Once-daily single-inhaler triple versus dual therapy in patients with COPD. N Engl J Med 2018; 378:1671-1680.
7. Sing D, Corradi M, Spinola M, et al. Triple therapy in COPD: new evidence with the extrafine fixed combination of beclamethasone dipropionate, formoterol fumarate and glycopyrronium bromide. Internal J Chronic Obstr Pulm Dis 2017; 12:2917-2928.
8. SPC TRIMBOW. Souhrn údajů o přípravku – SÚKL: trimbow-epar-product-information_cs.pdf.
9. SPC Trelegy Elipta. Souhrn údajů o přípravku – SÚKL: trelegy-ellipta-epar-product-information_cs.pdf.
10. Pauk N. Fixní trojkombinace flutikason furoát/umeklidinium/ vilanterol v terapii chronické obstrukční plicní nemoci. Farmakoterapie 2016; 12:500-504.
11. Virchow JC, Kuna P, Paggiaro P, et al. Single inhaler extrafine triple therapy in uncontrolled asthma (TRIMARAN and TRIGGER): two double-blind, parallel-group, randomised, controlled phase 3 trials. Lancet Respir Med 2019; 394:1737-49.
12. Singh D, Virchow JC, Canonica GW, et al. Extrafine triple therapy in patients with asthma and persistent airflow limitation. Eur Respiratory J 2020; 56(3):2000476.
13. Usmani OS, Singh D, Spinola M, et al. The prevalence of small airways disease in adult astma: A systematic literature review. Respiratory Med 2016; 116:19-27.
14. SPC Enerzair Breezhaler – SÚKl: enerzair-breezhaler-epar-product-information_cs.pdf.
15. Kerstjens HAB, Maspero J, Chapman KR, et al. Once-daily, single-inhaler mometason-indacaterol-glycopyrronium versus mometasone-indacaterol or twice-daily fluticasone-salmeterol in patients with inadequately controlled asthma (IRIDIUM): a randomised, double-blind, controlled phase 3 study. Lancet Respiratory Med 2020; 8(10):1000-1012, https://doi.org/10.1016/ S2213-2600(20)30190-9
16. Gessner C, Kornmann O, Maspero J, et al. Fixed-dose combination of indacaterol/glycopyrronium/mometasone furoate once-daily versus salmeterol/fluticasone twice-daily plus tiotropium once-daily in patients with uncontrolled asthma: A randomised, Phase IIIb, non-inferiority study (ARGON). Respiratory Med 2020; 170:106021.
17. Lee LA, Bailes Z, Barnes N, et al. Efficacy and safety of once-daily single-inhaler triple therapy (FF/UMEC/VI) versus FF/ VI in patients with inadequately controlled asthma (CAPTAIN): a double-blind, randomised, phase 3A trial. Lancet Respiratory Med 2021; 9:69–84.
18. La Force C, Feldman G, Spagethal S, et al. Efficacy and safety of twice-daily glycopyrrolate in patients with stable, symptomatic COPD with moderate-to-severe airflow limitation: the GEM1 study. Int J Chron Obstruct Pulmon Dis 2016; 11:1233-1243.
19. Marel M. Glykopyrronium bromid – nové anticholinergikum v léčbě chronické obstrukční plicní nemoci. Remedia 2013; 23:229-233.
MUDr. Alena Vlachová
Plicní klinika 2.LF a FN Motol V Úvalu 84, 150 09 Praha 5 e-mail:alena.vlachova@gmail.com
Obdrženo: 5. 5. 2021 Revidováno: 10. 5. 2021 Přijato k tisku: 18. 5. 2021



